-
Die Universität
- Herzlich willkommen
- Das sind wir
- Medien & PR
-
Studium
- Allgemein
- Studienangebot
- Campusleben
-
Forschung
- Profil
- Infrastruktur
- Kooperationen
- Services
-
Karriere
- Arbeitgeberin Med Uni Graz
- Potenziale
- Arbeitsumfeld
- Offene Stellen
-
Diagnostik
- Patient*innen
- Zuweiser*innen
-
Gesundheitsthemen
- Gesundheitsinfrastruktur
Forschungsteam Kwapiszewska
Forschungsschwerpunkt Chronische Atemwegs- und Lungenerkrankungen
Teamleiterin: Grazyna Kwapiszewska
Fokus: Lungengefäßerkrankungen besitzen eine multifaktorielle Pathobiologie, charakterisiert durch Veränderungen in den Zellen der Glatten Muskulatur, der Adventitia und des Endothels. Diese pathologischen Veränderungen bewirken einen Umbau des Lungenkreislaufs und eine massive Veränderung des Lumens von mittelgroßen und kleinen Lungenarterien. In den letzten Jahren haben sich die Behandlungsmethoden durch einen tiefgreifenden Umdenkungsprozess gewandelt, von Gefäße erweiternde über den Gefäßumbau entgegenwirkenden bis zu die Gefäße in den ursprünglichen Zustand zurückbildenden (sog. “reverse-remodelling”) Strategien. Ausgelöst wurde dieser Trend durch neue Forschungsergebnisse, die darauf schließen lassen, dass das proliferative und anti-apoptotische Geschehen in der Gefäßwand von mittelgroßen und kleinen Lungenarterien einige Merkmale mit Neoplasie, der Neubildung von Körpergeweben,gemeinsam hat. Die Ziele dieser Arbeitsgruppe sind die Entschlüsselung der molekularen und zellulären Mechanismen, die der Pathobiologie des pulmonalen Gefäßumbaus zugrunde liegen - wie z.B. Dysregulation in der extrazellulären Matrix, Transkriptionsfaktoren, die zu der anormalen Zellproliferation führen.
Vernetzung: Das LBI-LVR arbeitet sehr eng mit präklinischen (Akos Heinemann, Herbert Strobl, Gerald Höfler, Dagmar Kolb) und Klinischen Abteilungen (Jörg Lindenmann) zusammen. Die Abteilung für Pneumologie ist ein integrativer Teil des LBI-LVR. Das Forschungsteam zeichnet sich durch teamübergreifende Vernetzung und enge Kooperation mit dem Ludwig-Boltzmann-Institut für Lungengefäßforschung aus.
Projekte
Disturbed basement membrane and its proteolytic products drive vascular remodelling
- Die extrazelluläre Matrix (ECM) hat sich zunehmend als ein aktiver Treiber der Krankheitsprogression herausgestellt. Wir haben gezeigt, dass Basalmembrankomponenten bei verschiedenen Formen pulmonaler Gefäßerkrankungen differenziell reguliert werden. Hier werden wir untersuchen, wie die Störung der Basalmembran-Homöostase, pulmonale Erkrankungen verursacht oder verschlimmern kann und funktionell aktive ECM-abgeleitete Fragmente, Matrikine, freisetzt, die die vaskuläre Dysfunktion weiter vorantreibt.
- Projektdauer: 2017-2024
- Gefördert durch: Ludwig Boltzmann Institut für Lungengefäßforschung
- Projektpartner*innen: Wilhelm Bloch (German Sports University Cologne, Germany), Jochen Wilhelm (Universities of Giessen and Marburg Lung Center, Germany), Malgorzata Wygrecka (Universities of Giessen and Marburg Lung Center, Germany), Dagmar Kolb (Gottfried Schatz Research Center), Liliana Schaefer (Johann Wolfgang Goethe-Universität Frankfurt am Main, Germany)
Distinct cell subpopulations and their regulators drive specific features of vascular and parenchymal remodeling
- Zelluläre Heterogenität mit ihrer funktionellen Spezialisierung und Koordination sind Schlüsseldeterminanten für eine normale vaskuläre und parenchymale Lungenfunktion. Wir haben bereits berichtet, dass wichtige Zelltypen ihre Identität mit unterschiedlichen Eigenschaften während des Lungenumbaus bewahren. Diese Veränderungen im Zellschicksal führen zu dysfunktionalem Zellverhalten und beeinträchtigen direkt die vaskuläre und parenchymale Struktur und Funktion der Lunge. In diesem Projekt werden wir die Mechanismen untersuchen, die zelluläre Schicksalsentscheidungen bestimmen, sowie die zugrundeliegenden Regulatoren der phänotypischen Veränderungen, die mit Lungenerkrankungen einhergehen.
- Projektdauer: 2019-2022
- Gefördert durch: Ludwig Boltzmann Institut für Lungengefäßforschung
- Projektpartner*innen: Vinicio A de Jesus Perez (Stanford University, USA), Saverio Bellusci (Universities of Giessen and Marburg Lung Center, Germany), Elie El Agha (Institute for Lung Health, Germany), You-Yang Zhao (Feinberg School of Medicine, Northwestern University, USA)
Pulmonary arterial endothelial cell subpopulations in vascular remodeling processes in pulmonary hypertension
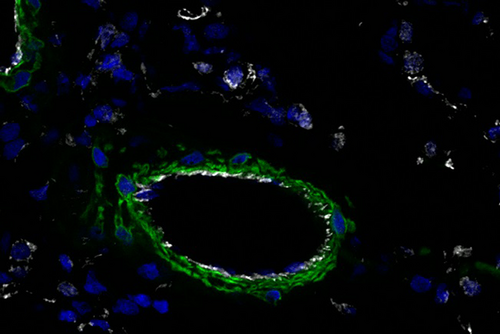
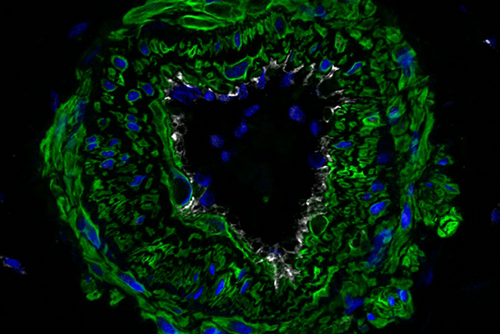
- Ein Ungleichgewicht in der Produktion von vasokonstriktorischen und vasodilatierenden Verbindungen durch Endothelzellen (EC) ist eine der frühesten pathologischen Veränderungen, die mit pulmonalen Gefäßerkrankungen assoziiert sind. Zusätzliche Studien weisen auf weitere Merkmale der EC-Dysfunktion hin, wie z.B. die erhöhte EC-Apoptose und die Hyperproliferation der verbleibenden apoptoseresistenten Zellen, als ein wichtiger Pathomechanismus im vaskulären Remodeling und der Entwicklung der pulmonalen Hypertonie. Unser Ziel ist es, Endothelzell-Subpopulationen und ihren Beitrag zum pulmonalen Gefäßremodeling zu identifizieren.
- Projektdauer: 2019-2022
- Gefördert durch: FFG-Österreichische Forschungsförderungsgesellschaft
- Projektpartner*innen: Ed Morrisey (Lung Biology Institute, University of Pennsylvania, USA)
Lehrstuhl für Physiologie & Pathophysiologie
Priv.-Doz.in Dr.in
Grazyna Kwapiszewska-Marsh
Grazyna Kwapiszewska-Marsh
T: +43 316 385 72057
Team
Mitarbeiter*innen
- Olschewski Andrea
- Biasin Valentina
- Birnhuber Anna
- Blanz Elisabeth
- Bonyadirad Ehsan
- Borek Izabela
- Bubalo Visnja
- Crnkovic Slaven
- Fliesser Elisabeth
- Halsegger Sabine
- Hrzenjak Andelko
- Jandl Katharina
- Mutgan Ceren
- Nagaraj Chandran
- Tischler Simone
- Treitler Alexandra Nina
- Valzano Francesco
- Zabini Diana
- Ziegler Hans Peter